Lipödeema on krooninen, etenevä rasvakudossairaus, joka vaikuttaa pääasiassa naisiin ja jolle on ominaista suhteeton rasvan kertyminen, kipu ja turvotus. Hormonaalisia vaihteluita raportoidaan usein oireiden laukaisijoina tai modulaattoreina, mutta ulkoisten hormonien, erityisesti hormonaalisten ehkäisyvälineiden, vaikutus on edelleen huonosti määritelty.
Tämän tutkimuksen tavoitteena oli selvittää hormonaalisen ehkäisyn käytön ja brasilialaisten naisten esiintymisen, vakavuuden ja itse raportoitujen lipödeemaoireiden pahenemisen välistä yhteyttä.
Menetelmät:
Tämä havainnoiva, poikkileikkaustutkimus toteutettiin Amato – Instituto de Medicina Avançadassa käyttäen rakenteellista verkkokyselyä, joka toteutettiin elokuun ja marraskuun 2025 välillä. Mukana oli 18-vuotiaita tai vanhempia Brasiliassa asuvia naisia, joilla epäiltiin tai vahvistettiin lipödeema, ja jotka antoivat sähköisen suostumuksen sekä suorittivat ydinosiot lipödeemaoireista, hormonihistoriasta ja ehkäisykäytöstä.
Kyselyt, joihin vastattiin alle 50 % ydinkysymyksistä, päällekkäiset merkinnät ja biologisesti epäuskottavat arvot jätettiin pois. Laskettiin oireiden (0–8) ja elämänlaadun (0–15) pisteet. Itse raportoidut oireiden muutokset hormonaalisen ehkäisyn aloittamisen jälkeen analysoitiin nelitasoisena muuttujana ja binäärisenä pahenevana muuttujana. Vapaa teksti sivuvaikutuksista ja alkamisen ajoituksesta luokiteltiin luonnollisen kielen käsittelyyn. Tilastollisiin analyyseihin kuuluivat khiinin neliötestit, Spearmanin korrelaatiot sekä logistiset ja lineaariset regressiot.
Tulokset:
Yhteensä 637 naista otettiin mukaan (keski-ikä 41,8±8,7 vuotta; keskimääräinen painoindeksi (BMI) 28,9±6,4 kg/m²); 77,1 %:lla oli vahvistettu lipedema-diagnoosi ja 92,3 % oli hormonaalisten ehkäisyvalmisteiden nykyisiä tai aiempia käyttäjiä. Käyttäjistä 58,8 % ilmoitti oireiden pahenevan ehkäisyn aloittamisen jälkeen (34,5 % vakavaa; 24,3 % lievää), 40,3 % ei kertonut muutosta ja 0,9 % parantumisesta (p<0,001). Vapaatekstianalyysi osoitti, että 15,1 % raportoi lipedemaoireiden alkavan ajallisesti, kun ehkäisy aloitetaan. Monimuuttujaanalyysissä korkeampi lähtöoirepiste oli vahvin riippumaton ennustaja pahenemiselle, kun taas ehkäisyn kesto ei liittynyt riskiin. Kivun voimakkuus ja BMI olivat tärkeimmät riippumattomat elämänlaadun vaikutuksen ennustajat.
Johtopäätökset:
Tässä suuressa otoksessa brasilialaisista naisista, joilla oli epäilty tai vahvistettu lipödeema, hormonaalisten ehkäisyjen käyttö liittyi usein itse raportoituun oireiden pahenemiseen, ja merkittävä vähemmistö raportoi oireiden alkavan ehkäisyn aloittamisen yhteydessä. Naiset, joilla oli korkeampi perusoireiden taakkaa, vaikuttivat erityisen haavoittuvilta. Nämä havainnot tukevat yksilöllistä ehkäisyneuvontaa raskaödeemaa sairastaville naisille ja korostavat tarvetta prospektiivisille tutkimuksille, joissa on objektiivisia mittareita syy-seuraussuhteiden ja mekanismien selkeyttämiseksi.
Johdanto
Lipödeema on krooninen, etenevä ihonalaisen rasvakudoksen sairaus, jota esiintyy lähes yksinomaan naisilla ja jolle on ominaista symmetrinen, kivulias rasvan kertyminen raajoissa, johon liittyy turvotusta, lisääntynyttä herkkyyttä ja vastustuskykyä painonpudotukseen [1,2]. Arvioitu esiintyvyys naisilla on 12,3 %, ja lipödeema rasittaa merkittävästi elämänlaatua ja toimintakykyä sairastuneilla [3].
Lipödeeman etiologia on edelleen epätäydellisesti selvitetty. Todisteet viittaavat geneettiseen osaan ja naisten sukupuolihormonien säätelevään rooliin, sillä tauti ilmenee tai pahenee usein hormonaalisten vaihteluiden aikana (murrosikä, raskaus, vaihdevuodet). Erityisesti hormonaaliset ehkäisymenetelmät on anekdoottisesti yhdistetty oireiden pahenemiseen, vaikka vahvaa tieteellistä näyttöä on vähän [4,5].
Tämän yhteyden biologinen uskottavuus perustuu useisiin mekanismeihin. Hormonaalisten ehkäisyvalmisteiden estrogeeniset komponentit voivat voimistaa syöttösolujen aktivaatiota, muuttaa verisuonten läpäisevyyttä, heikentää imusuoniston toimintaa ja vaikuttaa adiposyyttien lisääntymiseen. Lisäksi yleiset sivuvaikutukset, kuten painonnousu ja nesteen kertyminen, voivat pahentaa kliinisiä oireita [6,7].
Brasiliassa, jossa hormonaalinen ehkäisy on yleistä ja lipödeemaa ei ole diagnosoitu, tämän yhteyden ymmärtäminen on erittäin kliinisesti ja kansanterveydellisesti merkityksellistä [8]. Tämä poikkileikkaustutkimus pyrki tutkimaan hormonaalisen ehkäisyn ja lipödeeman esiintymisen, vakavuuden ja etenemisen välistä yhteyttä 637 brasilialaisen naisen otoksessa, hyödyntäen innovatiivista menetelmällistä lähestymistapaa luonnollisen kielen käsittelyyn suurten kielimallien avulla laadullisen datan rikastamiseksi. Pyrimme kvantifioimaan tätä yhteyttä, tunnistamaan pahenemisen ennustajia, tutkimaan välimuotoja ja arvioimaan vaikutuksia elämänlaatuun, tarjoten todisteita turvallisemmasta ehkäisyneuvonnasta tässä haavoittuvassa väestössä.
Materiaalit ja menetelmät
Tämä havainnoiva poikkileikkaustutkimus perustui itse järjestettyyn verkkokyselyyn ja toteutettiin Amato – Instituto de Medicina Avançada -koulussa elokuusta marraskuuhun 2025. Kohderyhmään kuului Brasiliassa asuvia 18-vuotiaita tai vanhempia naisia, joilla oli epäilty tai vahvistettu lipödeema, ja jotka suostuivat osallistumaan sähköisesti. Kelpoiset osallistujat olivat naisia, jotka raportoivat joko aiemman lääketieteellisen diagnoosin lipödeemasta tai yhteensopivista oireista seulontakyselyn mukaan ja jotka olivat täyttäneet vähintään kyselyn keskeiset osiot lipödeemaoireista, hormonaalisesta ja lisääntymishistoriasta sekä hormonaalisten ehkäisyaineiden käytöstä.
Epätäydelliset kyselylomakkeet, joihin vastattiin alle 50 % ydinkysymyksistä, päällekkäiset merkinnät, jotka tunnistettiin IP-osoitteen ja aikaleiman perusteella, sekä tietueet, joiden arvot olivat selvästi virheellisiä tai sisäisesti ristiriitaisia, jätettiin analyysistä pois, esimerkiksi aikuisten mahdottomat iät, pituudet tai painot tai yhdistelmät, kuten kuukautisikä, joka on suurempi kuin nykyinen ikä, tai negatiiviset ehkäisyajan käyttöajat. Osallistujien rekrytointi toteutettiin levittämällä kyselylinkkiä sosiaalisen median alustoilla, kuten Instagramissa, Facebookissa ja WhatsAppissa, lipödeemaa sairastavien naisten tukiryhmien, erikoisklinikoiden ja vastaanottojen sekä potilasyhdistysten kautta. Sisällyttämis- ja poissulkemiskriteerien soveltamisen jälkeen lopullinen analyyttinen otos koostui 637 osallistujasta.
Tätä tutkimusta varten käytettiin erityisesti kehitettyä jäsennelmän kyselylomaketta, joka koostui kahdeksasta osasta.
Osio A keräsi demografisia tietoja, kuten iän, painon, pituuden ja maantieteellisen sijainnin, ja esitti tietoon perustuvan suostumuslomakkeen.
Osio B sisälsi yhdeksän lipödeeman seulontakysymystä, joissa tutkittiin jalkakipua, etenevää turvotusta päivän aikana, oireiden pahenemista kuumuuden myötä, kosketusherkkyyttä, helppoja mustelmia, epäsuhtaista rasvan jakautumista, jalkojen koon vastustuskykyä ruokavaliolle ja liikunnalle, sukuhistoriaa, joka viittaa lipödeemaan, sekä oireiden alkamisen ajoitusta.
Osio C arvioi lipödeeman diagnoosia ja kliinisiä ominaisuuksia ja sisälsi tietoja diagnoosin lääketieteellisestä vahvistuksesta, diagnoosipäivästä, vastuullisen lääkärin erikoisalasta, lipödeeman vaiheesta 1–4, lipödeeman tyypistä I–IV sekä niihin liittyvistä sairauksista.
Osio D keräsi tietoa hormonaalisesta ja lisääntymishistoriasta, mukaan lukien kuukautisikä, kuukautiskierron säännöllisyys, raskauksien ja keskenmenojen määrä, vaihdevuodet, hormonikorvaushoidon käyttö sekä itse ilmoitetut kilpirauhasen muutokset.
Osio E, joka oli tämän tutkimuksen pääpaino, sisälsi 14 ehkäisyn käyttöä koskevaa kysymystä. Hormonaalinen ehkäisyaltistus luokiteltiin kolmeen toisensa poissulkevaan kategoriaan: nykyinen käyttäjä, joka määriteltiin käyttämään mitä tahansa hormonaalista ehkäisyä kyselyn aikaan; edellinen käyttäjä, joka määriteltiin käyttäneen hormonaalisia ehkäisyvälineitä aiemmin, mutta lopettaneen ne kokonaan; Eikä koskaan käytä sitä. Näissä tuotteissa arvioitiin nykyisen käyttötilanne, ehkäisymenetelmän tyyppi kuten pilleri, kohdunsisäinen laite (IUD), implantti, emättimen rengas tai injektio, tuotteen kaupallinen nimi, nykyinen ja kokonaiskäyttöaika, iän käytön alkaessa, jatkuvan ja keskeytetyn käytön mallin, lopettamisen syitä, koettuja sivuvaikutuksia, lipödeeman pahenemisen koetta ehkäisyn aloittamisen jälkeen, erityiset muutokset oireissa, painonnousu ja käytetyt vaihtoehtoiset ehkäisymenetelmät. Lopettamisen syitä kysyttiin vain aiemmilta käyttäjiltä. Osio F arvioi lipödeeman vaikutusta elämänlaatuun kysymyksillä, kuten liikkumisrajoitteita, arjen vaikeuksia, vaikutteita työhön, sosiaalisia ja emotionaalisia vaikutuksia, visuaalista analogista kipuasteikkoa 0–10, unen laatua, itsetuntoa neljän pisteen Likert-asteikolla ja vaihtoehdoilla erinomaiset, hyvät, kohtuulliset ja matalat, sekä perheen tuen havaitsemista.
Osio G tutki nykyisiä hoitoja, kuten imusolmukkeiden poistoa, kompressiota, fysioterapiaa, ravitsemus- ja psykologista seurantaa sekä lipödeemaleikkausta sekä tyytyväisyyttä näihin hoitoihin.
Lopuksi osio H mahdollisti lisähavainnot vapaan tekstin alalla ja kysyi, olivatko osallistujat kiinnostuneita saamaan tutkimuksen tulokset. Kyselylomakkeen koko rakenne, englanniksi käännettynä, esitetään liitteissä.
Ensisijainen tulosmuuttuja oli itse raportoitu lipödeeman paheneminen, joka liittyi hormonaalisen ehkäisyn käyttöön. Tämä kirjattiin neljän kategorian asteikolla, jossa vastevaihtoehdoissa ei havaittu eroa, kyllä hieman, kyllä, vakava paheneminen ja parantuminen. Pääanalyyseissä johdimme myös binäärisen tuloksen, joka vertasi minkä tahansa pahenemisen astetta, yhdistäen kategoriat kyllä hieman ja kyllä vakava paheneminen verrattuna ei pahentumiseen tai paranemiseen, yhdistettynä havaittua eroa ja parantumista. Toissijaiset tulokset sisälsivät lipödeeman oirepisteet, elämänlaatuun vaikuttavan pisteen, kipuasteikon ja itsetunnon. Oirepisteet vaihtelivat 0:sta 8:aan ja se laskettiin jakoon B kahdeksan seulontakysymyksen myönteisten vastausten summana, joissa arvioitiin kipua, turvotusta, kuumuuden myötä pahenemista, kosketusherkkyyttä, helppoa mustelmien syntymistä, suhteettoman rasvan kertymistä, jalkojen koon vastustuskykyä ruokavaliolle ja liikunnalle sekä perheen historiaa. Korkeammat arvot viittasivat suurempaan oirekuormaan. Elämänlaadun vaikutuspisteet vaihtelivat 0:sta 15:een, ja se laskettiin viiden kohdan painotettuna summana osiossa F, jotka arvioivat liikkumisrajoituksia, vaikeuksia päivittäisissä toiminnoissa, työllistymisvaikutuksia, sosiaalisia vaikutuksia ja tunnevaikutusta, ja korkeammat pisteet heijastivat suurempaa toimintakyvyn heikkenemistä. Kivun voimakkuutta arvioitiin numeerisella asteikolla nolla, eli ei kipua, 10:een, eli maksimikipuun. Itsetuntoa arvioitiin yllä kuvatulla Likert-tyyppisellä tehtävällä.
Hormonaalisiin ehkäisymenetelmiin liittyviä keskeisiä selittäviä muuttujia olivat nykyinen vs. aiempi vs. ei koskaan käytetty, käytetyn ehkäisyn tyyppi, käytön kesto vuosissa sekä käytön alkamisikä. Kovariaatioihin kuuluivat ikä vuosina, painoindeksi (BMI) kilogrammoina neliömetriä kohden, kuukautisikä, kuukautisajan jälkeen, itse ilmoitettujen samanaikaisten sairauksien määrä, lipeödeeman vaihe ja tyyppi sekä nykyiset lipedeeman hoidot.
Raakadataa käsiteltiin monivaiheisesti. Aluksi tehtiin puhdistus ja validointi, mukaan lukien kaksoiskappaleiden poisto IP-osoitteen ja aikaleiman perusteella sekä yhdenmukaisuustarkistukset muuttujien välillä. Kyselylomakkeet, joissa ydinosioista puuttuu laajasti ja jotka määriteltiin alle 50 % vastatuista ydinkysymyksistä, oli jo suljettu pois kelpoisuusvaiheessa kuten yllä on kuvattu. Jäljelle jäävissä asiakirjoissa puuttuvat arvot käsiteltiin konservatiivisesti. Johdetut muuttujat, kuten lipeturmaoireiden pistemäärä, vastaavat oireiden vakavuuskategoriat (lievä, keskivaikea, vaikea, erittäin vaikea) ja elämänlaatuun vaikuttava piste laskettiin vain, kun kaikki vaaditut pisteet olivat saatavilla ja muuten ne puuttuivat. Datan imputointia ei tehty, ja kaikki kuvailevat analyysit ja regressiomallit käyttivät saatavilla olevaa tapausmenetelmää, jolloin jokainen analyysi sisälsi kaikki osallistujat, joilla oli päteviä tietoja kyseisille muuttujille.
Näiden vaiheiden jälkeen laskettiin johdetut muuttujat analysoitavaksi. BMI laskettiin painona jaettuna pituuden neliöllä ja luokiteltiin Maailman terveysjärjestön kriteerien mukaan [9]. Ikä luokiteltiin viiden vuoden kategorioihin kuvailua varten. Lipödeemin oirepisteet ja elämänlaatuun vaikuttavat pisteet laskettiin kuten aiemmin kuvattiin. Hormonaalisen ehkäisyn käytön kesto kerättiin alun perin vapaan tekstin kentänä kohtaan E. Tietokäsittelyn aikana nämä vastaukset jäsenneltiin ja muunnettiin numeeriseksi muuttujaksi, joka ilmaisi kokonaiskäyttöajan vuosina, ja jota käytettiin jatkuvana ennustajana kuvailevissa ja monimuuttujaisissa analyyseissä.
Laadullisen tiedon rikastamiseksi datan rikastaminen suoritettiin luonnollisen kielen käsittelyllä paikallisella kielimallilla, joka toteutettiin LM Studiossa (Element Labs, Inc., Austin, Texas, Yhdysvallat) openai/gpt-oss-20b -mallilla. Vapaatekstikentät käsiteltiin sivuvaikutusten automaattiseen luokitteluun kahdeksaan ennalta määriteltyyn luokkaan. Painonnousu tarkoitti mitä tahansa itse raportoitua painonnousua, joka johtuu ehkäisyvälineiden käytöstä. Mielialan vaihtelut sisälsivät affektiivisia oireita, kuten ärtyneisyyttä, tunne-elämän vaihtelua, ahdistusta tai masentunutta mielialaa. Päänsärkyyn kuului raportteja päänsärystä, joka liittyi ehkäisyyn ajallisesti liittyvistä päänsärkyistä tai migreenistä. Pahoinvointi peitti pahoinvointia, oksentelua tai muuta yläruoansulatuskanavan epämukavuutta. Alentunut libidolla tarkoitettiin seksuaalisen halun tai seksuaalisen toimintahäiriön vähenemistä. Turvotus sisälsi raportteja jalkojen tai kehon turvotuksesta tai turvotuksesta. Verenvuoto tarkoitti poikkeavaa kohdun verenvuotoa, kuten tiputtelua, läpivuotoa tai muutoksia kuukautisten vuotokuviossa. Sivuvaikutukset, jotka eivät selvästi sopineet näihin kategorioihin, kuten akne tai rintojen arkuus, luokiteltiin jäännös”-kategoriaan. Samaa lähestymistapaa käytettiin hoitojen erottamiseen ja luokitteluun kategorioihin kuten ruokavalio, liikunta, kompressio, imusuoniston poisto, lääkkeet, kirurgia ja fysioterapia. Käsittelyyn kuului myös niihin liittyvien samanaikaisten sairauksien tunnistaminen ja standardointi sekä oireiden alkamisen ajallinen luokittelu kategorioihin kuten murrosikä, raskaus, vaihdevuodet ja ehkäisy. Satunnaisotos, joka koostui noin 10 % automaattisesti kategorioiduista vastauksista, tarkistettiin manuaalisesti kliinikon toimesta johdonmukaisuuden ja tarkkuuden varmistamiseksi, ja kehotteet hiottiin iteratiivisesti tarpeen mukaan.
Tilastolliset analyysit tehtiin käyttäen Python versiota 3.11 (Python Software Foundation, Wilmington, Delaware, Yhdysvallat) pandas-, numpy-, scipy-, statsmodels- ja scikit learn -paketeilla. Kuvailevassa analyysissä jatkuvat muuttujat tiivistettiin keskiarvoksi ja keskihajonnaksi sekä mediaani- ja kvartiliväliseksi vaihteluväliksi, kun taas kategoriset muuttujat esitettiin absoluuttisina ja suhteellisina taajuuksina. Jakauman normaaliutta arvioitiin Shapiro-Wilk -testillä. Päättelyanalyyseissä käytettiin khiinin neliö -testejä kategoristen muuttujien välisten yhteyksien selvittämiseksi, kahden ryhmän vertailuun Student-t-testejä tai Mann-Whitney U -testejä, ja varianssianalyysiä tai Kruskal-Wallis-testejä sovellettiin kolmen tai useamman ryhmän vertailuun tarpeen mukaan. Spearmanin korrelaatiokertoimet laskettiin arvioimaan jatkuvien muuttujien välisiä yhteyksiä. Monimuuttuja-analyysiä varten sovitettiin logistinen regressiomalli tunnistamaan ehkäisymenetelmien aiheuttamiin pahenemistekijöihin. Tämän mallin riippuvainen muuttuja oli binäärinen heikkenevä tulos, ja riippumattomia muuttujia olivat ikä, BMI, kuukautisikä, ehkäisyn kesto, oirepisteet ja samanaikaisten sairauksien määrä. Tulokset esitettiin todennäköisyyssuhteina 95 %:n luottamusväleillä. Lisäksi sovellettiin monilineaarinen regressiomalli tunnistamaan elämänlaadun vaikutuspisteisiin liittyvät tekijät. Tässä mallissa riippuva muuttuja oli elämänlaatuun vaikuttava piste, ja riippumattomia muuttujia olivat ikä, BMI, oirepisteet, kipuasteikko, ehkäisyvälineiden pahenemisen aste ja samanaikaisten sairauksien määrä. Tulokset esitettiin standardoituina beetakertoimina. Kaikissa analyyseissä otettiin 5 %:n merkitsevyystaso kaksihännän testeillä, ja p-arvoja säädettiin useissa vertailuissa Bonferronin menetelmällä tarvittaessa. Kaikki analyysit tehtiin käytettävissä olevalla tapausmenetelmällä, jolloin jokainen malli sisälsi kaikki osallistujat, joilla oli päteviä tietoja asiaankuuluvista muuttujista.
Tutkimus toteutettiin Helsingin julistuksen eettisten periaatteiden ja Brasilian asetusten mukaisesti, mukaan lukien kansallisen terveysneuvoston päätöslauselmat 466/2012 ja 510/2016. Kaikki osallistujat antoivat sähköisen tietoisen suostumuksen luettuaan kyselylomakkeen alussa esitetyn tietoon perustuvan suostumuslomakkeen. Tiedot anonymisoitiin ja tallennettiin turvallisesti AES 256 -salauksella. Tutkimusprotokolla hyväksyttiin Amato-instituutin eettisen komitean toimesta (hyväksyntänumero: 90936425.0.0000.0081). Anonymisoitu aineisto ja analyysien jäljentämiseen käytetty koodi ovat tekijöiden käytettävissä kohtuullisen pyynnön mukaisesti, Brasilian tietosuojaohjeiden mukaisesti.
Tulokset
Tutkimukseen osallistui yhteensä 637 naista, mikä on suurin brasilialainen otos, jota on tähän mennessä tutkittu lipödeemään. Demografiset ja kliiniset ominaisuudet paljastivat keskimääräiseksi iän 41,8±8,7 vuotta (vaihteluväli: 19–68 vuotta) ja keskimääräiseksi BMI:ksi 28,9±6,4 kg/m², ja suurimmalla osalla osallistujista (77,1 %; n=491) oli terveydenhuollon ammattilaisen vahvistama lipedema-diagnoosi. Maantieteellinen jakauma osoitti osallistujien enemmistöä Kaakkois-Englannista (64,8 %), jota seurasi etelä (16,6 %), mikä heijastaa sekä erikoistuneiden lipödeemahoitokeskusten alueellista keskittymistä että Brasilian väestön demografista jakautumista. Otoksen yksityiskohtaiset demografiset ja kliiniset ominaisuudet on esitetty taulukossa 1.
| Muuttuja | Arvo |
| Ikä (vuodet) | |
| Mean±SD | 41,8±8,7 |
| Mediaani (IQR) | 42.0 (35.0-47.0) |
| Min-max | 18-73 |
| BMI (kg/m²) | |
| Mean±SD | 28.9±6.4 |
| Mediaani (IQR) | 27.7 (24.8-32.0) |
Taulukko 1: Tutkimukseen osallistuneiden demografiset ja kliiniset ominaisuudet (n=637)
Data esitetään jatkuville muuttujille keskiarvona, mediaanina (IQR) ja alueena (mini±max) ja kategorisille muuttujille n (%).
SD: keskihajonta; IQR: kvartiilien välinen alue; BMI: kehon painoindeksi
Lipödeeman kliinisten ominaisuuksien osalta taudin vaiheiden jakautuminen osoitti, että vaihe 2 oli yleisin (32,2 %; n=205), jota seurasivat vaihe 1 (17,7 %; n=113) ja vaihe 3 (16,6 %; n=106), ja vaihe 4 edustaa 3,3 % (n=21); 12,4 % (n=79) ilmoitti ”En tiedä”. Yleisin lipedematyyppi oli tyyppi III, joka vaikutti lonkkiin, reisiin ja pohkeisiin (58,1 %; n=285), ja sitä seurasi tyyppi II, joka koski lonkkia ja reisiä (32,9 %; n=161). Merkittävä osa osallistujista raportoi samanaikaisia sairauksia, joista kilpirauhasen vajaatoiminta oli yleisin (28,1 %; n=179), jota seurasi ahdistus/masennus (22,6 %; n=144) ja verenpainetauti (18,5 %; n=118). Niihin liittyvien sairauksien taakka oli huomattava, mediaani oli kaksi samanaikaista sairautta per osallistuja. Lipödeeman kliiniset ominaisuudet otoksessamme on kuvattu taulukossa 2.
| Ominaisuudet | n (%) |
| Vahvistettu diagnoosi | |
| Kyllä | 491 (77.1%) |
| Epäilty | 131 (20.6%) |
| Ei | 15 (2.4%) |
| Lipödeeman vaihe | |
| Vaihe 2 | 205 (32.2%) |
| Vaihe 1 | 113 (17.7%) |
| Vaihe 3 | 106 (16.6%) |
| Ei tiedä | 79 (12.4%) |
| Vaihe 4 | 21 (3.3%) |
| Oirepisteet (0-8) | |
| Mean±SD | 6.07±1.54 |
Taulukko 2: Lipedeeman kliiniset ominaisuudet ja taudin vaikeusaste (n=637)
Data esitetään kategorisille muuttujille n (%) ja jatkuville muuttujille keskiarvo±SD. Prosenttiosuudet eivät välttämättä ole 100 % puuttuvan datan tai pyöristyksen vuoksi.
SD: keskihajonta
Hormonaalisen ehkäisyn käytön malli tutkimusväestössä osoitti, että 588 osallistujalla (92,3 %) oli nykyistä tai aiempaa kokemusta hormonaalisesta ehkäisystä. Ehkäisykokemusta omaavien joukossa yleisimmin raportoitu ehkäisytyyppi oli suun kautta otettavat tabletit (59,7 %; n=380), jota seurasivat hormonaalinen kierukka (13,7 %; n=87), suun kautta otettavat tabletit + hormonaalinen kierukka (5,5 %; n=35), pistos (2,7 %; n=17) ja implantti (2,2 %; n=14); Osallistujat saattoivat raportoida useammasta ehkäisytyypistä ajan myötä. Käytön mediaanikesto oli 7 vuotta (IQR: 3–15 vuotta), keskimäärin 10,3±9,1 vuotta, mikä viittaa merkittävään pitkäaikaiseen altistumiseen ulkoisille hormoneille tässä väestössä. Ehkäisyn alkamisen ikä oli keskimäärin 20,7±5,6 vuotta, tyypillisesti samaan aikaan lisääntymiskypsyyden kanssa. Nykyisten käyttäjien keskuudessa jatkuvat käyttötavat olivat hallitsevia (67,4 %), kun taas 32,6 % ilmoitti keskeytyneistä käyttöajoista. Hormonaalisen ehkäisyn kattava käyttömalli on esitetty taulukossa 3.
| Muuttuja | n (%) |
| Käyttötila | |
| Edellinen käyttäjä | 382 (60%) |
| Nykyinen käyttäjä | 230 (36.1%) |
| Ei koskaan käytetty | 25 (3.9%) |
| Ehkäisytyyppi*† | |
| Suun kautta otettava pilleri | 380 (59.7%) |
| Hormonaalinen kierukka | 87 (13.7%) |
| Suun kautta otettava pilleri + hormonaalinen kierukka | 35 (5.5%) |
| Injektio | 17 (2.7%) |
| Implantti | 14 (2.2%) |
Taulukko 3: Hormonaalisen ehkäisyn käytön malli ja tyyppi tutkimukseen osallistujien keskuudessa (n=637)
*Käytön kesto raportoitu 588 osallistujalle, joilla oli nykyinen tai aiempi ehkäisykokemus.
†Näytetään vain viisi yleisimmin raportoitua ehkäisytyyppiä; Osallistujat, jotka käyttivät erilaisia menetelmiä ajan myötä, voivat raportoida useita ehkäisytyyppejä.
Kierukka: kohdunsisäinen laite
Yksi tämän tutkimuksen kliinisesti merkittävimmistä havainnoista oli hormonaalisen ehkäisyn käytön yhteydessä esiintyvä lipödeeman oireiden pahenemisen esiintyvyys. 588 ehkäisyä käyttäneestä osallistujasta 346 (58,8 %) ilmoitti kokeneensa jonkin verran oireiden pahenemista. Erityisesti 203 osallistujaa (34,5 %) raportoi vakavaa pahenemista, kun taas 143 (24,3 %) havaitsi lievää pahenemista. Vain 237 osallistujaa (40,3 %) ei havainnut oireiden eroa, ja huomionarvoista on, että vain viisi osallistujaa (0,9 %) raportoi paranemista. Tämä vastausten jakauma on kuvattu taulukossa 4 ja visuaalisesti esitetty kuvassa 1. Tämän yhteyden tilastollinen merkittävyys vahvistettiin khiinin neliötestauksella, joka osoitti, että vasteiden jakauma poikkesi selvästi odotetusta yhtenäisestä jakaumasta (χ²=213,71; p<0,001), mikä osoittaa selvästi, että pahenemisen havainto ei ollut satunnainen ilmiö.
| Vastaanotto | n (%) |
| Eroa ei havaittu | 237 (40.3%) |
| Kyllä, vakava paheneminen | 203 (34.5%) |
| Kyllä, hieman | 143 (24.3%) |
| Parannettu | 5 (0.9%) |
Taulukko 4: Hormonaalisen ehkäisyn käytön yhteydessä koettujen lipedeemojen oiremuutosten jakautuminen (n=588)
Tiedot kattavat 588 osallistujan vastauksia, joilla oli nykyinen tai aiempi ehkäisykokemus. Kokonaisraportoituja pahenemisen astetta: 346 (58,8 %). Jakauma poikkeaa merkittävästi yhtenäisestä odotuksesta (χ²=213,71; p<0,001).
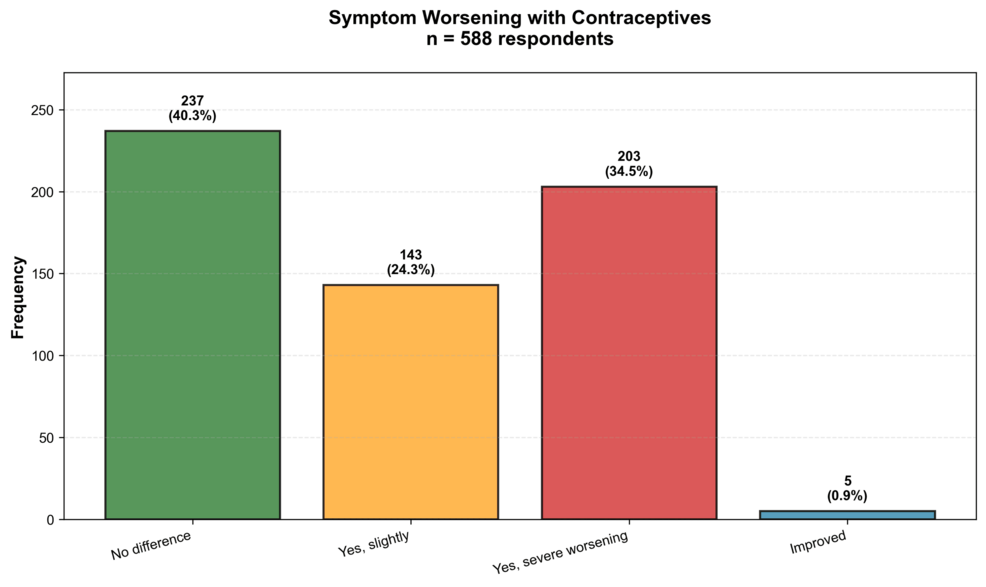
Kuva 1: Koettujen lipödeemaoireiden muutosten jakautuminen hormonaalisen ehkäisyn käytön yhteydessä (n=588)
Suurin osa osallistujista (58,8 %) ilmoitti jonkin verran pahenemista: 34,5 % vakavaa ja 24,3 % lievää. Vain 40,3 % ei huomannut eroa, ja 0,9 % ilmoitti parannuksesta.
Erityisen mielenkiintoinen ajallinen havainto syntyi vapaan tekstin analyysistä luonnollisen kielen käsittelyn avulla. Kun osallistujilta kysyttiin lipödeeman oireiden alkamisen ajoituksesta, 15,1 % (n=96) ilmoitti nimenomaan, että oireet alkoivat samanaikaisesti ehkäisyn aloittamisen kanssa, mikä viittaa mahdolliseen ajalliseen yhteyteen, joka vaatii jatkotutkimusta. Tämä havainto on esitetty kuvassa 2, jossa osoitetaan, että vaikka murrosikä pysyi oireiden yleisimpänä alkamisajana (39,7 %; n=253), ehkäisykausi oli kolmanneksi yleisimmin raportoitu laukaisujakso määrittelemättömän ajan (28,1 %; n=179) ja raskautta edeltävän (11,6 %; n=74) sekä vaihdevuosien (5,5 %; n=35) jälkeen.
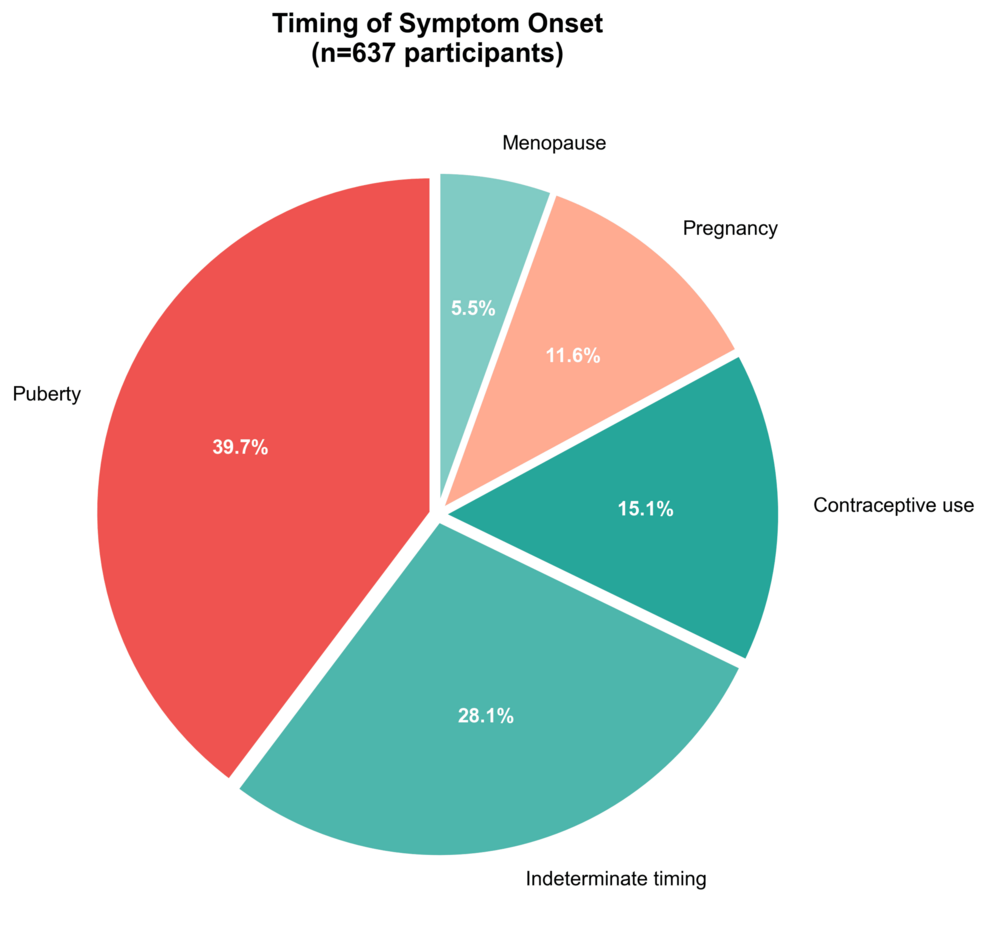
Kuva 2: Lipödeeman oireiden alkamisen ajallinen jakautuminen (n=637)
Murrosikä oli yleisin alkuvaihe (39,7 %), jota seurasi määrittelemätön ajankohta (28,1 %). Ehkäisyn käyttö (15,1 %), raskaus (11,6 %) ja vaihdevuodet (5,5 %) raportoitiin myös laukaisujaksoiksi.
Ymmärtääksemme paremmin ehkäisyyn liittyvän pahenemisen mekanismit, analysoimme tiettyjen sivuvaikutusten ja oireiden pahenemisen välistä yhteyttä. Yleisimmin raportoituja sivuvaikutuksia olivat painonnousu (41,8 %; n=266), turvotus (40,5 %; n=258), päänsärky (22 %; n=140) ja mielialan muutokset (13,2 %; n=84), kuten kuvassa 3 on esitetty. Tärkeää on, että nämä sivuvaikutukset osoittivat merkittäviä yhteyksiä lipödeeman pahenemiseen. Naiset, joilla oli painonnousua ehkäisynä sivuvaikutuksena, raportoivat huomattavasti todennäköisemmin lipödeeman pahenemista (71,7 %) verrattuna niihin, joilla ei ollut painonnousua (43,5 %), mikä tarkoittaa kliinisesti merkittävää eroa, 28,2 prosenttiyksikköä (χ²=29,32; p<0,0001). Samoin mielialan muutokset sivuvaikutuksena liittyivät korkeampiin oireiden pahenemisprosenttiin (77,4 % verrattuna 51,3 % ilman mielialan muutoksia; χ²=14,23; p=0,0002).
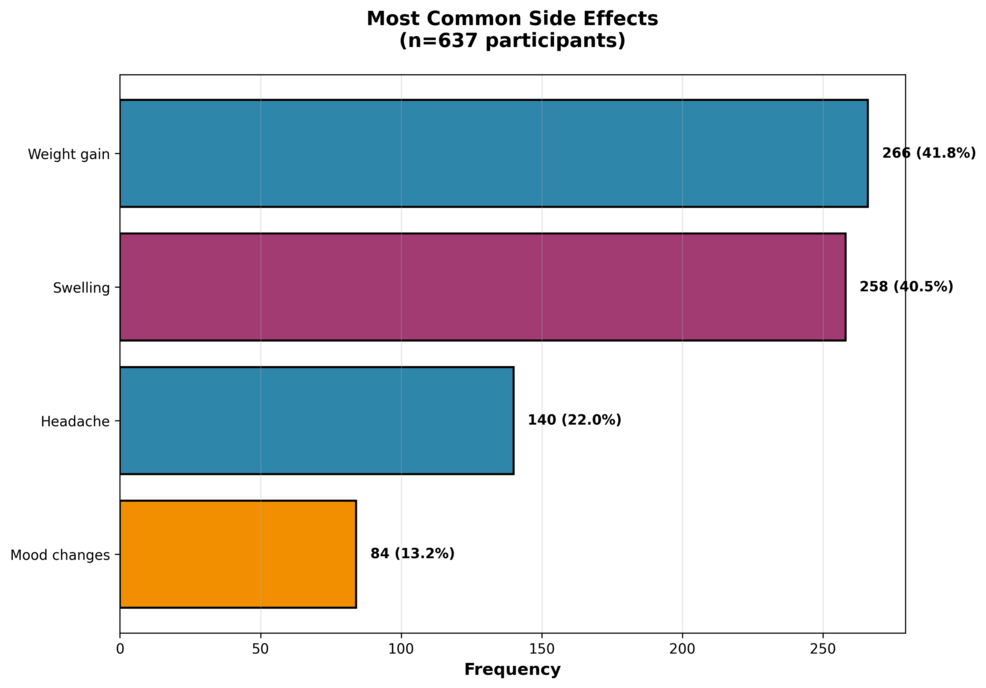
Kuva 3: Yleisimmin raportoitujen haittavaikutusten esiintyvyys hormonaalisen ehkäisyn aikana (n=637)
Painonnousu (41,8 %) ja turvotus (40,5 %) olivat yleisimmät haittavaikutukset, joita seurasivat päänsärky (22 %) ja mielialan muutokset (13,2 %).
Lipödeeman vaikutus elämänlaatuun oli merkittävä ja objektiivisesti mitattavissa. Kipuasteikko (välillä 0–10) antoi keskimääräisen pistemäärän 5,2±2,6, mediaani 5,00, mikä viittaa kohtalaiseen tai vaikeaan krooniseen kipuun tässä väestössä. Elämänlaatuun vaikuttava piste (välillä 0–15) oli keskiarvo 3,09±1,89, mediaani 3,00. Itsetunnon arviointi osoitti huomattavaa psykososiaalista kuormitusta, ja 70,5 % osallistujista raportoi joko kohtuullisen (38,3 %; n=244) tai matalan (32,2 %; n=205) itsetunnon olevan, kun taas vain 22,3 % ilmoitti hyvää tai erinomaista itsetuntoa. Nämä havainnot on tiivistetty taulukkoon 5.
| Muuttuja | Arvo |
| Kipuasteikko (0-10) | |
| Mean±SD | 5.2±2.6 |
| Mediaani | 5.00 |
| Elämänlaadun vaikutuspisteet (0–15) | |
| Mean±SD | 3.09±1.89 |
| Mediaani | 3.00 |
| Itsetunto, n (%) | |
| Reilua | 244 (38.3%) |
| Matala | 205 (32.2%) |
| Hyvä | 128 (20.1%) |
| Erinomaista | 14 (2.2%) |
Taulukko 5: Kivun voimakkuus, elämänlaadun vaikutus ja itsetunto tutkimuksen osallistujien keskuudessa
Kipuasteikko vaihtelee 0:sta (ei kipua) aina 10:een (maksimikipu) [10,11]. Elämänlaatuvaikutuspisteet vaihtelevat 0:sta (ei vaikutusta) 15:een (maksimivaikutus), lasketaan painotettuna summana liikkuvuusrajoitteiden, työkyvyn vaikutuksen, sosiaalisen vaikutuksen, tunnevaikutusten ja päivittäisten aktiivisuusvaikeuksien osalta [10]. Otoskoot vaihtelevat puutteellisten vastausten vuoksi: kipuasteikko n=559, elämänlaatuvaikutuspisteet n=310 ja itsetunto n=591.
SD: keskihajonta
Korrelaatioanalyysit paljastivat useita tilastollisesti merkitseviä yhteyksiä keskeisten muuttujien välillä (Taulukko 6). Kuten odotettua, ikä osoitti erittäin vahvaa korrelaation kuukautisvuosien kanssa (r=0,973; p<0,0001). Kliinisesti merkittävämpää on, että BMI osoitti kohtalaisen positiivisen korrelaation elämänlaatuvaikutuspisteen (r=0,313; p<0,0001) kanssa, mikä viittaa siihen, että korkeampi BMI liittyy suurempaan toimintakyvyn heikentymiseen. Oirepisteet osoittivat kohtalaista korrelaation kipuasteikkoon (r=0,431; p<0,0001), ja erityisesti kipuasteikko itsessään osoitti vahvinta yhteyttä elämänlaatuun vaikuttavaan (r=0,500; p<0,0001), mikä osoittaa, että kivun voimakkuus on ensisijainen tekijä toiminnallisissa rajoituksissa lipedeemaa sairastavilla naisilla.
| Muuttuja 1 | Muuttuja 2 | r | P-arvo | n |
| Ikä | Vuodet menarkin jälkeen | 0.973 | <0.0001 | 637 |
| BMI | Elämänlaadun vaikutuspisteet | 0.313 | <0.0001 | 637 |
| Oirepisteet | Kipuasteikko (F6) | 0.431 | <0.0001 | 559 |
| Kipuasteikko (F6) | Elämänlaadun vaikutuspisteet | 0.500 | <0.0001 | 559 |
Taulukko 6: Merkittäviä korrelaatioita keskeisten kliinisten muuttujien välillä (Spearmanin järjestyskorrelaatio)
Näytetään vain korrelaatioita r>0.3:n ja p<0.05:n kanssa. Korrelaation vahvuuden tulkinta: r=0,3-0,5 (kohtalainen); r=0,5-0,7 (vahva); ja r>0.7 (erittäin vahva).
BMI: kehon painoindeksi; F6: kysymys F6 tutkimuslomakkeesta (kipuasteikko 0-10)
Tunnistaaksemme riippumattomia lipödeeman pahenemisen ennustajia, jotka liittyivät ehkäisyyn ja mahdollisia sekoittavia tekijöitä, teimme monimuuttujaisen logistisen regressioanalyysin 568 osallistujalla, joilla oli täydelliset tiedot. Malli osoitti maltillista kokonaisistuvuutta (Pseudo R²=0,048; Akaiken informaatiokriteeri (AIC)=752.0; Bayesilainen informaatiokriteeri (BIC)=782,4), mikä viittaa siihen, että ehkäisyyn liittyvä paheneminen johtuu useista tekijöistä, jotka eivät ole tässä tutkimuksessa mitattuja. Taulukossa 7 esitetyt tulokset osoittivat, että oirepisteet olivat vahvin riippumaton pahenemisen ennustaja (OR=1,562; 95 % CI: 1,300-1,877; p<0,0001), mikä viittaa siihen, että jokainen yhden pisteen nousu lähtöoireiden vakavuudessa liittyi 56 %:n kasvuun ehkäisyyn liittyvän pahenemisen todennäköisyydessä. Tämä havainto viittaa siihen, että naiset, joilla on vakavammat aiemmat oireet, ovat erityisen alttiita hormonaalisille pahenemisvaiheille.
| Muuttuja | TAI | 95 % CI | P-arvo |
| Ikä | 0.926 | 0.776-1.105 | 0.3949 |
| BMI | 0.819* | 0.680-0.988 | 0.0369 |
| Ikä menarkiassa | 0.746* | 0.591-0.941 | 0.0135 |
| Käyttöaika (vuodet) | 0.931 | 0.789-1.100 | 0.4018 |
| Oirepisteet | 1.562* | 1.300-1.877 | <0.0001 |
| Samanaikaisten sairauksien määrä | 0.904 | 0.759-1.076 | 0.2572 |
Taulukko 7: Monimuuttujainen logistinen regressiomalli lipödeeman pahenemisen ennustajille ehkäisyhoidon myötä (n=568)
Riippuvainen muuttuja: oireiden paheneminen (kyllä/ei) ehkäisyn käytön aikana. Kaikki jatkuvat muuttujat standardoitiin ennen analyysiä. Mallin sovitus: Pseudo R²=0.048; AIC=752.0; BIC=782,4. *p<0.05. Otos sisältää vain osallistujia, joilla on täydelliset tiedot kaikista mallimuuttujista.
OR: kertoimien suhde; CI: luottamusväli; BMI: kehon painoindeksi; AIC: Akaiken informaatiokriteeri; BIC: Bayesilainen informaatiokriteeri
Mielenkiintoista on, että kaksi muuta muuttujaa osoittivat merkittäviä mutta suojaavia yhteyksiä. Kuukautisikä osoitti suojaavaa vaikutusta (OR=0,746; 95 % CI: 0,591-0,941; p=0,0135), mikä viittaa siihen, että myöhemmin alkaneilla kuukautisillä saattavilla naisilla saattoi olla vähentynyt alttius ehkäisyyn liittyvälle pahenemiselle. BMI osoitti myös maltillista suojaavaa yhteyttä (OR=0,819; 95 % CI: 0,680-0,988; p=0,0369), mikä on hieman vastoin intuitiota osoittava havainto, joka saattaa heijastaa valintaharhaa tai mittaamatonta sekoittamista ja vaatii lisätutkimuksia. Huomionarvoista on, että ehkäisyn kesto ei ollut merkittävästi yhteydessä pahenemiseen (OR=0,931; 95 % CI: 0,789-1,100; p=0,4018), mikä viittaa siihen, että oireiden paheneminen saattaa liittyä yksilölliseen alttiuteen eikä kumulatiiviseen hormonaaliseen altistukseen. Ikä tai samanaikaisten sairauksien määrä eivät osoittaneet merkittäviä yhteyksiä pahenemiseen säädetyn mallin mukaan.
Täydentääksemme ymmärrystämme lipödeeman toiminnallisista vaikutuksista suoritimme useita lineaarisia regressioita tunnistaaksemme elämänlaadun heikentymisen ennustajia 310 osallistujalla täydellisillä tiedoilla. Malli selitti 29,5 % elämänlaadun pisteiden vaihtelusta (R²=0,295; korjattu R²=0,281; F(6,303)=21,16; s<0.001). Kuten taulukossa 8 osoitetaan, kipuasteikko nousi hallitsevaksi ennustajaksi (β=0,641; 95 % CI: 0,454-0,827; p<0,0001), ja standardoidut kertoimet osoittivat, että kivun voimakkuus oli ylivoimaisesti elämänlaatuun vaikuttava tekijä. BMI oli toinen merkitsevä ennustaja (β=0,364; 95 % CI: 0,194-0,535; p<0,0001), mikä viittaa siihen, että kehon koostumus itsenäisesti vaikuttaa toiminnallisiin rajoituksiin oireiden vakavuuden korrelaation lisäksi. Huomionarvoista on, että ehkäisymenetelmien heikkenemisen aste ei osoittautunut merkittäväksi elämänlaadun vaikutuksen ennustajaksi sekoittavien tekijöiden (β=0,106; 95 % CI: -0,054–0,266; p=0,1943), mikä viittaa siihen, että hormonaaliset vaikutukset oireisiin voivat vaikuttaa elämänlaatuun täydentävien reittien kautta, joita ensisijaisesti välittää kipu ja kehon koostumus suoran itsenäisen vaikutuksen kautta.
| Muuttuja | β (standardoitu) | 95 % CI | P-arvo |
| Ikä | 0.061 | -0,105:stä 0,226:een | 0.4718 |
| BMI | 0.364* | 0,194–0,535 | <0.0001 |
| Oirepisteet | 0.044 | -0,137–0,225 | 0.6346 |
| Kipuasteikko (F6) | 0.641* | 0,454–0,827 | <0.0001 |
| Ehkäisyn pahenemisen aste | 0.106 | -0,054:stä 0,266:een | 0.1943 |
| Samanaikaisten sairauksien määrä | 0.078 | -0,085–0,240 | 0.348 |
Taulukko 8: Moninkertainen lineaarinen regressiomalli elämänlaadun vaikutusten ennustajille (n=310)
Riippuva muuttuja: elämänlaatuun vaikuttava pistemäärä (0–15 pistettä). Kaikki jatkuvat muuttujat standardoitiin ennen analyysiä. Mallin istuvuus: R²=0,295; korjattu R²=0,281; F(6,303)=21,16; p<0.001. *p<0.05. Otos sisältää vain osallistujia, joilla on täydelliset tiedot kaikista mallimuuttujista.
β: standardoitu regressiokerroin; CI: luottamusväli; BMI: kehon painoindeksi
Yhteenvetona nämä havainnot osoittavat merkittävän ja kliinisesti merkityksellisen yhteyden hormonaalisen ehkäisyn käytön ja lipödeeman oireiden pahenemisen välillä merkittävällä osalla käyttäjistä, ja oireiden vakavuus, kuukautisikä sekä erityiset sivuvaikutukset (erityisesti painonnousu ja mielialan muutokset) toimivat tärkeinä modulaatiotekijöinä. Elämänlaatuun kohdistuva vaikutus välittyy ensisijaisesti kivun voimakkuuden ja BMI:n kautta, ja krooninen kipu on tärkein muokattavissa oleva kohde terapeuttisille toimenpiteille. Oireiden puhkeamisen ja ehkäisyhoidon aloittamisen ajallinen yhteensattuma 15,1 %:lla osallistujista yhdistettynä korkeaan havaittuun pahenemisen esiintyvyyteen viittaa siihen, että ulkoiset hormonit voivat olla tärkeässä roolissa sekä lipödeeman ilmenemisoireiden laukaisemisessa että etenemisessä, vaikka poikkileikkausrakenne estää lopullisen syy-seuraussuhteen.
Keskustelu
Tämä tutkimus, joka perustuu suurimpaan brasilialaiseen lipödemaa tutkintaan (n=637), tarjoaa vahvaa ja kliinisesti merkityksellistä näyttöä merkittävästä yhteydestä hormonaalisen ehkäisyn käytön ja lipödeemaoireiden pahenemisen välillä. Tämä korkea koetun pahenemisen esiintyvyys, tilastollisesti merkitsevä (s<0,001), vahvistaa aiempia kirjallisuusraportteja [2,4,5] ja muuttaa toistuvan kliinisen havainnon mitattavaksi tieteelliseksi löydökseksi, mikä viittaa siihen, että ulkoiset hormonit näyttelevät tärkeää roolia lipödeeman patogeneesissä ja etenemisessä [1].
Näiden tulosten analysoinnissa on olennaista erottaa suorat tilastolliset assosiaatiot laajemmista teoreettisista tulkinnoista. Tämän tutkimuksen tiedot tukevat vahvasti pääasiallista yhteyttä: korkeaa esiintyvyyttä (58,8 %) hormonaalisen ehkäisyn yhteydessä lipödeeman oireiden pahenemisen havaitsemisessa. Samoin regressiot tunnistavat kipuasteikon (β=0,641) ja BMI:n (β=0,364) hallitseviksi elämänlaadun negatiivisten vaikutusten ennustajiksi. Laajemmat selittävät teoriat, erityisesti ”tulehdusmalli”, tulisi kuitenkin pitää spekulatiivisina [1,12-14]. Tulkinta, että korrelaation puute käytön keston kanssa (p=0,4018) viittaa ”yksilölliseen alttiuteen” kumulatiivisen vaikutuksen sijaan, on toimiva hypoteesi, ei todistettu johtopäätös, koska tutkimuksessa ei mitattu objektiivisia tulehdus- tai imusuoniston biomarkkereita. Tämä selkeä ero tilastollisen assosiaation ja kausaalihypoteesin välillä on ratkaisevan tärkeä löydösten oikean tulkinnan kannalta.
Nämä havainnot vahvistavat hypoteesia, jonka mukaan lipödeema ei ole vain hormonaalisten tekijöiden muokkaamista, vaan myös tulehdus- ja imusuonereittien syvästi vaikutuksen alaisena, joissa ehkäisyvalmisteet toimivat kontekstuaalisina vahvistimina.
Mielenkiintoinen havainto oli, että 15,1 % osallistujista (n=96) raportoi, että lipödeemaoireiden alkaminen osui ajallisesti yhteen ehkäisyn alkamisen kanssa. Vaikka tämä havainto viittaa mahdolliseen ajalliseen yhteyteen, joka on yksi Bradford Hillin [15] syy-seuraussuhteen kriteereistä, on tärkeää korostaa, että poikkileikkaustutkimuksissa ei ole mahdollista erottaa (a) ehkäisyvälineitä laukaisevana tekijänä, (b) olemassa olevan subkliinisen sairauden paljastamista ja (c) muistiharhaa. Tulevaisuuden tutkimuksia tarvitaan tämän suhteen selkeyttämiseksi. Kun yhdistetään vahvaan annos-vaste-yhteyteen oirepisteiden ja pahenemisriskin välillä (OR=1,562; 95 % CI: 1,300–1,877; s<0,0001), jossa jokainen lisäoire lisäsi pahenemisriskiä 50 %, hypoteesi mahdollisesta mahdollisesta biologisista mekanismeista voisi välittyä yhteydestä vahvistuu [16,17], vaikka suoraa kausaalista vahvistusta ei olisi.
Merkittävä havainto oli, että ehkäisyn kesto ei ennustanut pahenemista (OR=0,931; p=0,4018), eikä ikä (OR=0,926; p=0,3949), mikä viittaa siihen, ettei haittavase noudata kumulatiivista annosriippuvaista kaavaa. Merkittäviä ennustajia olivat lähtötason oirepisteet (OR=1,562; p<0,0001), mikä viittaa siihen, että ennestään vakavuus määrittää alttiuden hormoneille, kun taas kuukautisikä (OR=0,746; p=0,0135) ja BMI (OR=0,819; p=0,0369) osoittivat maltillisia suojaavia vaikutuksia, mahdollisesti heijastaen eroja metabolis-hormonaalisessa ohjelmoinnissa. Mahdollinen tulkinta on, että ehkäisyn paheneminen voi heijastaa yksilöllistä alttiutta eikä annosriippuvaista vaikutusta, jossa altis naiset pahenevat varhain, kun taas ei-alttiit sietävät pitkäaikaista käyttöä. Vaihtoehtoisesti tämä havainto voi heijastaa selviytymisharhaa (naiset, joilla oireet pahenivat merkittävästi, lopettivat käytön varhain) tai riittämätöntä tilastollista kykyä havaita heikoja yhteyksiä. Se, että lähtöoireiden pistemäärä oli vahvin ennustaja (OR=1,562; s<0,0001), viittaa siihen, että sairauden ennestään olemassa oleva vakavuus saattaa vaikuttaa vasteeseen ulkoisiin hormoneihin, vaikka tarkka mekanismi on vielä selvittämättä. Tämä selittää, miksi vahvin ennustaja oli tarkalleen lähtöoireiden pistemäärä (OR=1,562; s<0,0001), joka on suora merkki aiemmasta tulehdustoiminnasta, ei altistuksen kesto. Kuukautisikä (OR=0,746; p=0,0135) toimii puolestaan ajallisena proxyna immunometaboliselle ohjelmoinnille: varhainen kuukautiset merkitsevät suurempaa tulehdusikkunaa kudosten kypsymisen aikana, mikä aiheuttaa kohonneen lähtötason reaktiivisuutta. Yhteenvetona voidaan todeta, että ehkäisyvalmisteisiin liittyvä lipödeema näyttää syntyvän hormonien vahvistamasta konstitutiivisesta haavoittuvuudesta, ei myrkyllisen kertymisen kautta, joka suuntaa kliinisen painopisteen käytön kestosta riskifenotyyppien varhaiseen tunnistamiseen.
Vasto intuitiivinen havainto ansaitsee korostaa: ehkäisyn kesto ei ollut merkittävä ennustaja monimuuttujaanalyysin pahenemiselle (OR=0,931; p=0,4018). Jos paheneminen olisi kumulatiivinen annosriippuvainen ilmiö, pidempi käyttöaika korreloi suuremman heikkenemisen todennäköisyyden kanssa. Tämän suhteen puuttuminen viittaa vaihtoehtoiseen mekanismiin: kumulatiivisen vaikutuksen sijaan vaikuttaa olevan yksilöllinen alttius, jossa haavoittuvaiset naiset pahenevat varhaisessa vaiheessa (mahdollisesti ensimmäisten syklien aikana), kun taas ei-alttiit voivat käyttää ehkäisyä loputtomasti ilman merkittävää heikkenemistä.
Sivuvaikutusten analyysi paljasti vahvan yhteyden painonnousun ja lipödeeman pahenemisen välillä (χ²=29,32; p<0,0001): 71,7 % painonnousua kokeneista naisista raportoi oireiden pahenevan, kun taas painonnousua ei ollut 43,5 %, ero on 28,2 prosenttiyksikköä. Tämä havainto sisältää useita tulkintoja. Ensinnäkin ehkäisyvalmisteiden aineenvaihdunnalliset ja nesteen kertymiseen liittyvät vaikutukset voivat pahentaa ennestään olemassa olevia lipödeemaoireita, luoden päällekkäisyyttä iatrogeenisten sivuvaikutusten (hormonien aiheuttama turvotus) ja taustalla olevan sairauden ilmenemismuotojen välillä [18-21]. Toiseksi painonnousu voi heijastaa yksilöllisen hormonaalisen vasteen merkkiä, jossa naiset, jotka ovat aineenvaihdunnallisesti herkemmät ehkäisylle, reagoivat myös enemmän rasvakudoksessa, johon lipödeema vaikuttaa [22-24]. Kolmanneksi käänteistä kausaalisuutta ei voida sulkea pois, sillä lipödeeman paheneminen (lisääntynyt turvotus ja kudostilavuus) tulkitaan osallistujien toimesta ”painonnousuksi”. Tutkimuksen poikkileikkaussuunnittelu ei mahdollista näiden hypoteesien erottamista, vaikka kaikki ovat biologisesti uskottavia eivätkä toisensa poissulkevia.
Mielialan muutos sivuvaikutuksena osoitti myös merkittävää yhteyttä lipödeeman pahenemiseen (77,4 % vs. 51,3 %; p=0,0002). Tätä havaintoa voidaan tulkita eri tavoin. Yksi mahdollisuus on, että mielialan muutokset heijastavat lisääntynyttä herkkyyttä ulkoisten hormonien systeemisille vaikutuksille, mikä voi viitata suurempaan yksilölliseen alttiuteen sekä keskushermostossa että muissa kohdekudoksissa, mukaan lukien rasvakudos [25,26]. Vaihtoehtoisesti naiset, joilla on vakavammat lipödeema-oireet, voivat aiheuttaa suuremman lähtötason psykologisen stressikuorman, mikä altistaa heidät ehkäisystä johtuville mielialan muutoksille, mikä edustaa sekoittavaa eikä suoraa syy-yhteyttä [3]. Lopuksi sekä mielialan oireisiin että lipödeeman pahenemiseen voivat vaikuttaa mittaamattomat muuttujat (kuten stressi, uni ja ruokavaliotekijät), mikä luo virheellisen yhteyden. Prospektiiviset tutkimukset, joissa on standardoitu psykometrinen arviointi ja hormonaalisen herkkyyden biologiset markkerit, ovat välttämättömiä tämän yhteyden luonteen selvittämiseksi.
Havaitun yhteyden laajuus on kliinisesti merkittävä: 588 hormonaalisen ehkäisyn käyttäjän joukossa 58,8 % raportoi oireiden pahenevan (χ²=213,71; p<0,001), jakauma poikkeaa merkittävästi satunnaisesta odotuksesta. Erityisen merkityksellistä on, että 15,1 % osallistujista (n=96) raportoi ehkäisyn alkamisen ja oireiden alkamisen ajallista yhteneväisyyttä, mikä viittaa mahdolliseen ajalliseen yhteyteen, joka ansaitsee prospektiivisen tutkimuksen.
Vaikka tämä tutkimus ei sisältänyt objektiivisia tulehduksen tai imusuonenhoidon mittauksia, tulokset ovat hämmästyttävän yhdenmukaisia kirjallisuudessa nousevien patofysiologisten mallien kanssa, jotka ehdottavat lipödeemaa pehmytkudosten krooniseksi tulehdukselliseksi oireyhtymäksi. Useat kirjoittajat ovat ehdottaneet integroitua tulehduksen → imusuonikon → rasvan mallia, jossa matalan asteen tulehdusprosessit edeltävät ja ylläpitävät taudin tunnusomaisia muutoksia [27,28].
Tässä käsitteellisessä viitekehyksessä syöttösolujen aktivaatio, verisuonten läpäisevyyden muutokset, etenevä imusuonen toimintahäiriö ja tulehdusvälittäjien (histamiini, tryptaasi, prostaglandiinit, sytokiinit) vapautuminen loisivat mikroympäristön, joka edistää suhteettoman suurta adiposyyttien hyperplaasiaa ja fibroosia [28-33]. Viimeaikaiset multi-omiikkatutkimukset ovat tunnistaneet tyypillisiä molekyylisignatuureja, kuten polarisoituneet M2-makrofagit, kohonnut CD163-ilmentyminen, interstitiaalinen hypoksia ja solunulkoinen matriisien uudelleenmuodostuminen metalloproteiiniaasien välityksellä [13,14,34].
Nämä havainnot tarkentavat ymmärrystämme ”immunologisesta suojasta” ja viittaavat siihen, että lipödeemakudoksen tarjoama suoja maksaa homeostaattisen hinnan. Tiedämme ”vaihdevuosien vaihdon” käsitteestä, että estrogeeni on elintärkeä ylläpitämään ”metabolisen sielun” suojaavaa toimintaa syöpää vastaan. Synteettisten hormonien käyttöönotto näyttää kuitenkin luovan paradoksin: ne ylläpitävät ”systeemisen suojan” signaalia, mutta ylikuormittavat paikallisen verisuonten ja imusuoniston kapasiteetin. Siksi hormoni ei ole pahis, vaan voimakas modulaattori, joka altistuneessa fenotyypissä voi kallistaa tasapainoa systeemisen immunometabolisen edun ja paikallisen oireiden mukavuuden välillä, mikä vaatii yksilöllistä kliinistä lähestymistapaa naisendokrinologian demonisoinnin sijaan [14,34-36].
Yhteys tutkimustulosten ja tulehdusmallin välillä
Useat tämän tutkimuksen havainnot, vaikka eivät todista tätä mallia, ovat yhdenmukaisia sen ennusteiden kanssa:
Ensinnäkin käytön keston vaikutuksen puuttuminen (OR=0,931; p=0,4018) on ristiriidassa kumulatiivisen hormonaalisen toksisuusmallin kanssa [37-39] ja viittaa yksilölliseen alttiuteen, mikä on yhteneväinen hypoteesin kanssa, jonka mukaan naiset, joilla on jo kohonnut kudoksen ”tulehdussävy”, reagoivat kielteisesti altistuksen alusta lähtien, riippumatta altistuksen kestosta.
Toiseksi, lähtöoireiden pistemäärä hallitsevana pahenemisen ennustajana (OR=1,562; p<0,0001) viittaa siihen, että aiempi sairauden aktiivisuus, mahdollinen epäsuora tulehdusprosessin merkki, määrittää alttiuden ulkoisille hormoneille.
Kolmanneksi, iän suojaava yhteys kuukautisaikaan (OR=0,746; p=0,0135) voi heijastaa eroja tulehdus- ja ”ohjelmoinnissa” kriittisten kehitysjaksojen aikana, vaikka vaihtoehtoisia tulkintoja (sekoittava, sattumanvarainen) ei voida sulkea pois [40-43]. Hypoteesi on, että myöhempi menarkki tarkoittaa vähemmän kumulatiivista altistumista estrogeenisille vaihteluille immuuni- ja verisuonijärjestelmien kypsymisen aikana ihon alaisissa rasvakudoksissa.
Neljänneksi yleisimmät sivuvaikutukset, nimittäin turvotus (40,5 %) ja painonnousu (41,8 %), ovat odotettavissa sekä tulehduksellisen nesteen kertymisen että suorien hormonaalisten vaikutusten ilmentymiä, mikä tekee syyn ja seurauksen erottelusta vaikeaa [18-21,44,45].
Hormonit modulaattoreina, eivät aiheuttajina
Tämä viitekehys viittaa siihen, että sukupuolihormonit, olivatpa ne endogeenisiä tai ulkoisia, eivät ole lipödeeman ensisijainen syy, vaan saavat modulaattoreita, jotka vahvistavat jo olemassa olevaa tulehdusherkkyyttä. Tämä selittäisi, miksi voimakkaan hormonaalisen vaihtelun (murrosikä, raskaus, ehkäisy, vaihdevuodet) virstanpylväät usein osuvat samaan aikaan oireiden alkamisen tai pahenemisen kanssa, ilman että ne ovat suoraa aiheuttajaa [3,46]. Estrogeenit ja progestogeenit säätelevät syöttösoluja, endoteelia ja imusuoniston toimintaa, vahvistaen jo valmiiksi toimintahäiriöille alttiita piirejä [47-49].
Evolutiivisen lääketieteen näkökulmasta arvellaan, että lipödeema saattaa edustaa haitallista reaktiota esi-isien suojaavista perifeeristen reserviohjelmista, kun kyseessä on nykyaikainen ympäristö, jolle on ominaista krooninen tulehdusaltistus (tulehdusta edistävä ruokavalio, istumatyö, ympäristön hormonihäiriötekijät, univaje). Tässä yhteydessä jatkuva eksogeeninen hormonaalinen altistus toimisi jo valmiiksi inflammoherkän fenotyypin vahvistajana [50].
Kriittiset rajoitukset ja tarve validoinnille
On välttämätöntä korostaa, että nämä tulkinnat ovat spekulatiivisia ja perustuvat kirjallisuuden synteesiin, eivät suoriin mittareihin. Tässä tutkimuksessa ei mitattu tulehdusbiomarkkereita (CRP, IL-6, TNF-α, tryptaasi), ei objektiivisesti arvioitu imusuonikkeiden toimintaa (lymfoskintografia, indosyaniinivihreä (ICG)), eikä tehty histopatologista tai molekyylianalyysiä. Lisäksi tämä tutkimus ei pysty erottamaan todellista pato-fysiologista lipödeeman pahenemista itsenäisistä sivuvaikutuksista (iatrogeeninen ödeema), joka tulkitaan sairauden pahenemiseksi.
Tästä syystä tulehdusmalli on edelleen houkutteleva ja biologisesti uskottava hypoteesi, mutta sitä ei ole vahvistettu tämän tutkimuksen aineistoilla.
Tulokset eivät ainoastaan selitä etiologisia näkökohtia, vaan niillä on myös suoria vaikutuksia kliiniseen käytäntöön ja terapeuttisten interventioiden suunnitteluun. Ennen ehkäisylääkkeiden aloittamista kliinikoiden tulisi aktiivisesti tutkia lipedeeman merkkejä validoiduilla seulontatyökaluilla, jotka on integroitu rutiininomaisiin gynekologisiin protokolliin. Naisille, joilla on vahvistettu tai epäilty lipedema, tulisi saada selkeää tietoa pahenemisriskistä, jotta voidaan valita harkittu valinta hormonaalisten ehkäisymenetelmien ja ei-hormonaalisten menetelmien välillä. Naisilla, joilla tilanne pahenee, voidaan harkita näyttöön perustuvia adjuvanttisia toimenpiteitä kroonisiin tulehdussairauksiin, kuten ravitsemuksen optimointiin, imusuonikkeisiin painottuviin liikuntaan ja elämäntapatekijöiden hallintaan. Lisäksi pitkittäistutkimukset, jotka testaavat tulehduksen palautuvuutta, sekä pragmaattisia tutkimuksia, joissa verrataan tulehduksen hallintaan keskittyviä strategioita, ovat tarpeen. Lopuksi varhaista ja objektiivista seurantaa suositellaan naisille, jotka päättävät jatkaa ehkäisyä riskistä huolimatta.
Kyselymme ei kuvannut progestogeenityyppiä riittävän yksityiskohtaisesti, jotta se tukisi alaryhmäanalyysejä tietyillä koostumuksilla; siksi emme voi tehdä johtopäätöksiä yksittäisistä progestogeeneista aineistomme perusteella. Siitä huolimatta, kun valitaan ehkäisyvalmistetta kroonista turvotusta ja kipua sairastaville naisille, kuten lipödemaa sairastaville, kliinikoiden tulisi ottaa huomioon kunkin valmisteen farmakologinen profiili ja tunnetut verisuoniriskit. Tässä yhteydessä drospirenonia sisältävät yhdistetyt suun kautta otettavat ehkäisyvalmisteet ansaitsevat erityistä varovaisuutta, sillä niiden erilaiset antimineralokortikoidivaikutukset ja antiandrogeeniset vaikutukset sekä vertailututkimuksissa raportoitu suurempi laskimotromboembolian riski, vaikka näitä tekijöitä ei suoraan arvioitu tässä analyysissä. Vahva näyttö suurista kohorttitutkimuksista ja meta-analyyseistä osoittaa, että drospirenonia sisältävät yhdistetyt ehkäisyvalmisteet liittyvät laskimotromboembolian riskiin, joka on noin 1,5–3 kertaa suurempi verrattuna toisen sukupolven levonorgestreeliä sisältäviin valmisteisiin [51-53]. Kun otetaan huomioon, että lipödeemaa sairastavilla naisilla on usein kohonneet lähtötason riskitekijät, kuten kohonnut BMI, laskimostasis ja lievä krooninen tulehdus, suuremman trombogeenisen potentiaalin sisältävän valmisteen lisääminen voi merkitä kliinisesti tarpeetonta riskin kasvua [3,29,54]. Siksi lipödemaa sairastavilla naisilla, jotka tarvitsevat hormonaalista ehkäisyä, on järkevää välttää drospirenonia sisältäviä valmisteita, kun turvallisempia vaihtoehtoja on saatavilla, ja priorisoida valmisteita, joilla on suotuisampi hemostaattinen profiili, kuten levonorgestreelia sisältävät yhdistetyt tabletit tai hormonittomat menetelmät.
Elämänlaadun heikkeneminen oli havaittavissa ja mitattavissa tutkitussa otoksessa. Monimuuttujainen lineaarinen regressioanalyysi osoitti, että tärkeimmät riippumattomat ennustajat elämänlaatuun suuremmalle vaikutukselle olivat kipuasteikko (β=0,641; p<0,0001) ja BMI (β=0,364; p<0,0001). Huomionarvoista on, että ehkäisymenetelmien heikkenemisen aste ei osoittautunut merkittäväksi ennustajaksi sekoittavien tekijöiden (β=0,106; p=0,1943) korjaamisen jälkeen, mikä viittaa siihen, että elämänlaatuun vaikuttaa ensisijaisesti kivun voimakkuus ja kehon koostumus riippumatta hormonaalisen heikkenemisen havaitsemisesta.
Psykososiaalinen vaikutus oli yhtä merkittävä: 70,5 % osallistujista ilmoitti matalasta tai kohtuullista itsetuntoa ja mediaanikipupisteiksi 5 asteikolla 0–10. Nämä tiedot korostavat lipödeeman aiheuttamaa kaksinkertaista rasitusta, fyysistä ja emotionaalista, jota hormonaalinen ehkäisy voi pahentaa, mikä korostaa tarvetta kokonaisvaltaiselle lähestymistavalle näiden potilaiden hoidossa [3,55,56].
Tämän tutkimuksen tärkeä metodologinen erottava tekijä oli innovatiivinen luonnollisen kielen käsittelyn käyttö paikallisen suuren kielimallin avulla, jolla systemaattisesti luokitellaan 19 vapaan tekstin muuttujaa, mukaan lukien sivuvaikutukset, hoidot, samanaikaiset sairaudet ja oireiden alkamisen ajoitus. Tämä lähestymistapa mahdollisti laadullisten tietojen kvantifioinnin, jotka perinteisesti katoavat perinteisissä tilastollisissa analyyseissä tai vaativat intensiivistä manuaalista luokittelua, mikä edusti merkittävää menetelmällistä edistysaskelta lipödeematutkimuksessa. Tarkka havaitseminen, että 15,1 % naisista yhdisti oireiden puhkeamisen erityisesti hormonaalisen ehkäisyn käyttöön, mahdollisti tällä tekniikalla, mikä korostaa sen merkitystä tärkeiden kliinisten vivahteiden havaitsemisessa.
Evoluution näkökulmasta lipödeema saattaa edustaa muinaisen suojaavan ääreisreserviohjelman nykyistä epäsopeutumista, joka tulehduksellisen ultra-altistuksen (pro-inflammatiivinen ruokavalio, dysbioosi ja aineenvaihdunnan endotokemia, ympäristön hormonihäiriköt, univaje/kronohäiriö, istuma-elämäntapa) jatkuvassa aktiivisena [50]. Ympäristön xenoestrogeenit, kuten bisfenoli A ja ftalaatit, toimivat kotekijöinä, jäljitellen estrogeenia ja pahentaen endoteelin ja syöttösolujen toimintahäiriöitä [57-59]. Jatkuva ulkoinen hormonaalinen altistus toimii modulaattorina, joka pahentaa tätä tulehduksellista-lymfaattista fenotyyppiä, ei välttämättä sen käynnistäjänä. Tässä kehyksessä lipedema ilmenee ohjelmoidun tulehdusalttiuden fenotyyppinä, johon hormonit vaikuttavat kontekstuaalisina vahvistimina. Potilaat usein mainitsevat lihasmassan kasvun ja painonlaskun vastustuskyvyn, joka heijastaa sitä, että kudos ei ole aineenvaihdunnallisesti normaalia rasvaa, vaan tulehtunutta ja fibroottista matriisiaa, joka on vastustuskykyinen perinteiselle lipolyosille [60,61].
Käytännössä tuloksemme osoittavat, että hormonaalisia ehkäisyä käyttävien lipödemaa sairastavien naisten joukossa suuremman lähtötason oireiden taakka raportoivat todennäköisemmin myöhemmästä pahenemisesta, vaikka iän, BMI:n ja samanaikaisten sairauksien huomioiminen on otettu huomioon. Vaikka poikkileikkausrakenne sulkee pois kausaalisen päättelyn, tämä johdonmukainen yhteys viittaa siihen, että tulehduksellisempi tai kipuherkistetty fenotyyppi voi olla erityisen altis ulkoisille hormonaalisille modulaatioille. Välitön kliininen seuraus on, että ehkäisyneuvonta lipödeemassa tulisi yksilöllistää – naisille, joilla on hyvin korkeat lähtötason oirepisteet, tulisi tiedottaa selkeästi pahenemisen mahdollisuudesta, seurata tarkemmin toimenpiteen aloittamisen jälkeen ja tarjota tarvittaessa hormonittomia vaihtoehtoja. Tulevaisuutta ajatellen, jos tulevat objektiiviset tulehdusmarkkerit sisältävät prospektiiviset tutkimukset vahvistavat, että tietyt tulehdusendotyypit ennustavat ehkäisymenetelmien oireiden pahenemista, kohdennettu ennakkoarviointi, jossa kliiniset oirepisteet yhdistetään valittuihin biomarkkereihin kuten hs CRP:hen tai lähtötryptaasiin, voisi auttaa tunnistamaan korkeamman riskin naisia ja ohjata henkilökohtaisempaa ehkäisymenetelmien valintaa. Monimodaalisia tulehdusta ehkäiseviä interventioita voitaisiin myös testata tulevissa tutkimuksissa, mukaan lukien strategiat, jotka yhdistävät tulehdusta ehkäiseviä ravintoja, syöttösolujen stabilointiaineita kuten ketotifeeniä tai kromoliinia, kohdennettuja lisäravinteita kuten kurkumiini, kversetiini tai palmitoyletanolamidi, unen optimointia sekä imusuonistumiseen keskittyvää liikuntaa [62-68]. Objektiivinen seuranta biomarkkereiden seurannalla ennen ja jälkeen interventioiden olisi välttämätöntä palautuvuuden arvioinnissa, ja riskin kerrostumista voitaisiin parantaa kehittämällä ennustavia pisteitä, jotka yhdistävät perusoireet, hormonihistorian ja tulehdusmarkkerit.
Tämä tutkimus esittää rajoituksia, jotka on otettava huomioon. Ensinnäkin poikkileikkaussuunnittelu ei mahdollista lopullisen kausaalisuuden määrittämistä, vaan ainoastaan ajallisen assosiaation. Toiseksi tiedot raportoidaan itse ilman objektiivista validointia antropometrisilla mittareilla, tulehdusbiomarkkereilla tai kuvantamistutkimuksilla, mikä tekee mahdottomaksi erottaa todellista patofysiologista lipedemaa ja itsenäisiä sivuvaikutuksia (iatrogeeninen nesteen kertyminen), jotka tulkitaan taustalla olevan sairauden pahenemiseksi. Kolmanneksi muistamisharha voi vaikuttaa muistiin oireiden alkamisen ajoituksesta ja lääkityksen käytöstä. Neljänneksi, tukiryhmistä rekrytoitu kätevä otos saattaa yliarvioida assosiaation (valintaharha). Lopuksi ehkäisyn tyypin, annostuksen tai annostelutavan mukaan ei voitu jakaa niitä eri tapaan. Näistä rajoituksista huolimatta suuri otoskoko (n=637), vahvat monimuuttujaanalyysit ja havaitun vaikutuksen laajuus (58,8 %) antavat havainnoille merkittävän pätevyyden.
On syytä tunnustaa tärkeä metodologinen rajoitus: ilman objektiivisia mittareita (tulehdusbiomarkkerit, lymfosintigrafia, pehmytkudosten ultraäänitutkimus) ei ole mahdollista kategorisesti erottaa (A) lipödeeman todellinen patofysiologinen heikkeneminen, (B) ehkäisyvalmisteiden itsenäiset sivuvaikutukset (iatrogeeninen nesteen kertyminen), joka virheellisesti tulkitaan taustalla olevan sairauden pahenemiseksi, ja (C) hypervigilanssiharhaa naisilla, joilla on jo vakavia oireita. Tulevissa tutkimuksissa tulisi sisällyttää objektiivisia päätepisteitä, eli standardoitujen ympärysmittajen vaihtelua, bioimpedanssin aiheuttamaa kehon vesiindeksiä, seerumin tryptaasin annostusta ja verisuonten läpäisevyysmarkkereita, jotta todellinen tulehdussignaali ja havaintokohina voidaan erottaa. Tämä varoitus ei kuitenkaan kumoa havaittua assosiaatiomallia, vaan vain vivahtaa sen mekanistista tulkintaa. Silti löydösten johdonmukaisuus useissa analyyseissä, ajallinen johdonmukaisuus ja havaittujen vaikutusten laajuus antavat tunnistetulle mallille epidemiologista uskottavuutta.
Prospektiiviset tutkimukset tulisi seurata naisia ennen ehkäisyn aloittamista objektiivisilla mittareilla (ympärysmitta, bioimpedanssi, tulehdusbiomarkkerit) ajallisen kausaliteetin selvittämiseksi. Kontrolloituja keskeytystutkimuksia tarvitaan oireiden palautumisen testaamiseksi hormonaalisen lopettamisen jälkeen, ja mieluiten vertaillaan myös multimodaalisia tulehduskipulääkkeitä faktoriaalisessa mallissa. Molekyylikarakterisointi ihonalaisen kudosbiopsian ja farmakogenomisten tutkimusten avulla voisi tunnistaa herkkyysfenotyypit ja tarkat terapeuttiset kohteet. Lopuksi ehkäisyn tyypin, annoksen ja annostelutavan mukaan kerrostaminen mahdollistaisi hormoniprofiilien tunnistamisen, joilla on vähemmän haitallinen vaikutus lipödemaa sairastavilla naisilla.
Johtopäätökset
Tämä tutkimus osoitti merkittävän ja kliinisesti merkityksellisen yhteyden hormonaalisen ehkäisyn käytön ja lipödeemaoireiden pahenemisen välillä. Tulokset ovat yhdenmukaisia hypoteesin kanssa, jonka mukaan eksogeeniset hormonit saattavat säädellä taudin kliinistä ilmentymistä alttiissa naisilla. Vaikka tarkat mekanismit ovat vielä selvittämättä, tiedot viittaavat siihen, että lähtötason oireiden pisteet ja lisääntymishistoria voivat vaikuttaa yksilön vasteeseen ehkäisyihin. Näillä havainnoilla on välittömiä vaikutuksia ehkäisyneuvontaan lipödeemaa sairastavilla naisilla, ja prospektiiviset tutkimukset objektiivisilla mittareilla ovat tarpeen kausaalisuuden ja mekanismien selvittämiseksi.
Lähteet
Kotanen-Polvilampi E. Asiantuntijablogi lipödeemasta ja hormonaalisen ehkäisyn yhteydestä. Lipelife.fi (2025). Saatavilla: https://www.lipelife.fi
- Herbst KL, Kahn LA, Iker E, et al.: Standard of care for lipedema in the United States. Phlebology. 2021, 36:779-96. 10.1177/02683555211015887
- Amato AC, Peclat AP, Kikuchi R, et al.: Brazilian Consensus Statement on lipedema using the Delphi methodology. J Vasc Bras. 2025, 24:e20230183. 10.1590/1677-5449.202301832
- Amato AC, Amato FC, Amato JL, Benitti DA: Lipedema prevalence and risk factors in Brazil. J Vasc Bras. 2022, 21:e20210198. 10.1590/1677-5449.202101981
- Kaftalli J, Bonetti G, Marceddu G, et al.: AKR1C1 and hormone metabolism in lipedema pathogenesis: a computational biology approach. Eur Rev Med Pharmacol Sci. 2023, 27:137-47. 10.26355/eurrev_202312_34698
- Torre YS, Wadeea R, Rosas V, Herbst KL: Lipedema: friend and foe. Horm Mol Biol Clin Investig. 2018, 33:10.1515/hmbci-2017-0076
- Amato AC, Amato LL, Benitti D, Amato JL: Assessing the prevalence of HLA-DQ2 and HLA-DQ8 in lipedema patients and the potential benefits of a gluten-free diet. Cureus. 2023, 15:e41594. 10.7759/cureus.41594
- Theoharides TC, Valent P, Akin C: Mast cells, mastocytosis, and related disorders. N Engl J Med. 2015, 373:163-72. 10.1056/NEJMra1409760
- Farias MR, Leite SN, Tavares NU, et al.: Use of and access to oral and injectable contraceptives in Brazil. Rev Saude Publica. 2016, 50:14s. 10.1590/S1518-8787.2016050006176
- Physical status: the use of and interpretation of anthropometry, report of a WHO expert committee. (1995). Accessed: September 10, 2025: https://www.who.int/publications/i/item/9241208546.
- Amato AC, Amato FC, Benitti DA, Dos Santos RV: Translation, cultural adaptation, and validation of a lipedema symptoms questionnaire. J Vasc Bras. 2020, 19:e20200049. 10.1590/1677-5449.200049
- Euasobhon P, Atisook R, Bumrungchatudom K, Zinboonyahgoon N, Saisavoey N, Jensen MP: Reliability and responsivity of pain intensity scales in individuals with chronic pain. Pain. 2022, 163:e1184-91. 10.1097/j.pain.0000000000002692
- Is lipedema a unique entity?. (2020). Accessed: 2025: https://vascular.cc/paper_artigo/is-lipedema-a-unique-entity/.
- Grewal T, Kempa S, Buechler C: Lipedema: a disease triggered by M2 polarized macrophages?. Biomedicines. 2025, 13:561. 10.3390/biomedicines13030561
- Wolf S, Rannikko JH, Virtakoivu R, et al.: A distinct M2 macrophage infiltrate and transcriptomic profile decisively influence adipocyte differentiation in lipedema. Front Immunol. 2022, 13:1004609. 10.3389/fimmu.2022.1004609
- Hill AB: The environment and disease: association or causation?. Proc R Soc Med. 1965, 58:295-300. 10.1177/003591576505800503
- Price TM, O’Brien SN, Welter BH, George R, Anandjiwala J, Kilgore M: Estrogen regulation of adipose tissue lipoprotein lipase-possible mechanism of body fat distribution. Am J Obstet Gynecol. 1998, 178:101-7. 10.1016/s0002-9378(98)70634-9
- Pedersen SB, Kristensen K, Hermann PA, Katzenellenbogen JA, Richelsen B: Estrogen controls lipolysis by up-regulating α2A-adrenergic receptors directly in human adipose tissue through the estrogen receptor α. Implications for the female fat distribution. J Clin Endocrinol Metab. 2004, 89:1869-78. 10.1210/jc.2003-031327
- Stachenfeld NS: Sex hormone effects on body fluid regulation. Exerc Sport Sci Rev. 2008, 36:152-9. 10.1097/JES.0b013e31817be928
- Stachenfeld NS, Keefe DL: Estrogen effects on osmotic regulation of AVP and fluid balance. Am J Physiol Endocrinol Metab. 2002, 283:E711-21. 10.1152/ajpendo.00192.2002
- Stachenfeld NS, Taylor HS: Effects of estrogen and progesterone administration on extracellular fluid. J Appl Physiol (1985). 2004, 96:1011-8. 10.1152/japplphysiol.01032.2003
- Stachenfeld NS, Taylor HS: Exogenous oestradiol and progesterone administration does not cause oedema in healthy young women. Clin Endocrinol (Oxf). 2007, 66:410-8. 10.1111/j.1365-2265.2007.02748.x
- Mayeda ER, Torgal AH, Westhoff CL: Weight and body composition changes during oral contraceptive use in obese and normal weight women. J Womens Health (Larchmt). 2014, 23:38-43. 10.1089/jwh.2012.4241
- Gallo MF, Grimes DA, Schulz KF, Helmerhorst FM: Combination estrogen-progestin contraceptives and body weight: systematic review of randomized controlled trials. Obstet Gynecol. 2004, 103:359-73. 10.1097/01.AOG.0000107298.29343.6a
- Rosenberg M: Weight change with oral contraceptive use and during the menstrual cycle: results of daily measurements. Contraception. 1998, 58:345-9. 10.1016/s0010-7824(98)00127-9
- Petersen N, Kearley NW, Ghahremani DG, Pochon JB, Fry ME, Rapkin AJ, London ED: Effects of oral contraceptive pills on mood and magnetic resonance imaging measures of prefrontal cortical thickness. Mol Psychiatry. 2021, 26:917-26. 10.1038/s41380-020-00990-2
- Pope CJ, Oinonen K, Mazmanian D, Stone S: The hormonal sensitivity hypothesis: a review and new findings. Med Hypotheses. 2017, 102:69-77. 10.1016/j.mehy.2017.03.012
- Kruglikov IL, Scherer PE: Is the endotoxin-complement cascade the major driver in lipedema?. Trends Endocrinol Metab. 2024, 35:769-80. 10.1016/j.tem.2024.04.004
- Felmerer G, Stylianaki A, Hollmén M, et al.: Increased levels of VEGF-C and macrophage infiltration in lipedema patients without changes in lymphatic vascular morphology. Sci Rep. 2020, 10:10947. 10.1038/s41598-020-67987-3
- Kruppa P, Gohlke S, Łapiński K, et al.: Lipedema stage affects adipocyte hypertrophy, subcutaneous adipose tissue inflammation and interstitial fibrosis. Front Immunol. 2023, 14:1223264. 10.3389/fimmu.2023.1223264
- Wilgus TA, Ud-Din S, Bayat A: A review of the evidence for and against a role for mast cells in cutaneous scarring and fibrosis. Int J Mol Sci. 2020, 21:9673. 10.3390/ijms21249673
- Hügle T: Beyond allergy: the role of mast cells in fibrosis. Swiss Med Wkly. 2014, 144:w13999. 10.4414/smw.2014.13999
- Ruoss SJ, Hartmann T, Caughey GH: Mast cell tryptase is a mitogen for cultured fibroblasts. J Clin Invest. 1991, 88:493-9. 10.1172/JCI115330
- Hirai S, Ohyane C, Kim YI, et al.: Involvement of mast cells in adipose tissue fibrosis. Am J Physiol Endocrinol Metab. 2014, 306:E247-55. 10.1152/ajpendo.00056.2013
- Straub LG, Funcke JB, Joffin N, et al.: Defining lipedema’s molecular hallmarks by multi-omics approach for disease prediction in women. Metabolism. 2025, 168:156191. 10.1016/j.metabol.2025.156191
- Amato A, Amato J, Benitti D: The lipedema phenotype is inversely associated with celiac disease autoimmunity: testing the immunological shield hypothesis in NHANES. medRxiv. 2025, 10.64898/2025.12.01.25341350
- Amato A, Amato J, Benitti D: Lipedema-like phenotype and cancer prevalence in US women: a cross-sectional analysis of NHANES 2011-2014. medRxiv. 2025, 10.64898/2025.12.02.25341445
- Bofill Rodriguez M, Yong LN, Mirkov S, Bekos C, Lethaby A, Farquhar C: Long-term hormone therapy for perimenopausal and postmenopausal women. Cochrane Database Syst Rev. 2025, 11:CD004143. 10.1002/14651858.CD004143.pub6
- Vinogradova Y, Coupland C, Hippisley-Cox J: Use of hormone replacement therapy and risk of breast cancer: nested case-control studies using the QResearch and CPRD databases. BMJ. 2020, 371:m3873. 10.1136/bmj.m3873
- Type and timing of menopausal hormone therapy and breast cancer risk: individual participant meta-analysis of the worldwide epidemiological evidence. Lancet. 2019, 394:1159-68. 10.1016/S0140-6736(19)31709-X
- Resztak JA, Choe J, Nirmalan S, et al.: Analysis of transcriptional changes in the immune system associated with pubertal development in a longitudinal cohort of children with asthma. Nat Commun. 2023, 14:230. 10.1038/s41467-022-35742-z
- Argente J, Dunkel L, Kaiser UB, Latronico AC, Lomniczi A, Soriano-Guillén L, Tena-Sempere M: Molecular basis of normal and pathological puberty: from basic mechanisms to clinical implications. Lancet Diabetes Endocrinol. 2023, 11:203-16. 10.1016/S2213-8587(22)00339-4
- Ning X, Huang Q, Guo D, Zhou Y, Li Y, Li X: The role of adipose tissue in puberty and reproductive health. Front Endocrinol (Lausanne). 2025, 16:1543787. 10.3389/fendo.2025.1543787
- Orsso CE, Colin-Ramirez E, Field CJ, Madsen KL, Prado CM, Haqq AM: Adipose tissue development and expansion from the womb to adolescence: an overview. Nutrients. 2020, 12:2735. 10.3390/nu12092735
- Oelkers WK: Effects of estrogens and progestogens on the renin-aldosterone system and blood pressure. Steroids. 1996, 61:166-71. 10.1016/0039-128x(96)00007-4
- Thomas W, Harvey BJ: Estrogen-induced signalling and the renal contribution to salt and water homeostasis. Steroids. 2023, 199:109299. 10.1016/j.steroids.2023.109299
- Child AH, Gordon KD, Sharpe P, Brice G, Ostergaard P, Jeffery S, Mortimer PS: Lipedema: an inherited condition. Am J Med Genet A. 2010, 152A:970-6. 10.1002/ajmg.a.33313
- Zaitsu M, Narita S, Lambert KC, et al.: Estradiol activates mast cells via a non-genomic estrogen receptor-α and calcium influx. Mol Immunol. 2007, 44:1977-85. 10.1016/j.molimm.2006.09.030
- Jensen F, Woudwyk M, Teles A, et al.: Estradiol and progesterone regulate the migration of mast cells from the periphery to the uterus and induce their maturation and degranulation. PLoS One. 2010, 5:e14409. 10.1371/journal.pone.0014409
- Narita S, Goldblum RM, Watson CS, Brooks EG, Estes DM, Curran EM, Midoro-Horiuti T: Environmental estrogens induce mast cell degranulation and enhance IgE-mediated release of allergic mediators. Environ Health Perspect. 2007, 115:48-52.
- Amato AC: The evolutionary theory of lipedema: a perspective on energy storage and chronic inflammation. Cureus. 2025, 17:e88809. 10.7759/cureus.88809
- Lidegaard Ø, Nielsen LH, Skovlund CW, Skjeldestad FE, Løkkegaard E: Risk of venous thromboembolism from use of oral contraceptives containing different progestogens and oestrogen doses: Danish cohort study, 2001-9. BMJ. 2011, 343:d6423. 10.1136/bmj.d6423
- Vinogradova Y, Coupland C, Hippisley-Cox J: Use of combined oral contraceptives and risk of venous thromboembolism: nested case-control studies using the QResearch and CPRD databases. BMJ. 2015, 350:h2135. 10.1136/bmj.h2135
- Gronich N, Lavi I, Rennert G: Higher risk of venous thrombosis associated with drospirenone-containing oral contraceptives: a population-based cohort study. CMAJ. 2011, 183:E1319-25. 10.1503/cmaj.110463
- Patton L, Ricolfi L, Bortolon M, Gabriele G, Zolesio P, Cione E, Cannataro R: Observational study on a large Italian population with lipedema: biochemical and hormonal profile, anatomical and clinical evaluation, self-reported history. Int J Mol Sci. 2024, 25:1599. 10.3390/ijms25031599
- Dudek JE, Białaszek W, Ostaszewski P: Quality of life in women with lipoedema: a contextual behavioral approach. Qual Life Res. 2016, 25:401-8. 10.1007/s11136-015-1080-x
- Dudek JE, Białaszek W, Ostaszewski P, Smidt T: Depression and appearance-related distress in functioning with lipedema. Psychol Health Med. 2018, 23:846-53. 10.1080/13548506.2018.1459750
- Valent P, Akin C, Bonadonna P, et al.: Mast cell activation syndrome: importance of consensus criteria and call for research. J Allergy Clin Immunol. 2018, 142:1008-10. 10.1016/j.jaci.2018.06.004
- Weinstock LB, Tenkhoff M, Gutovich J, Afrin LB: Imatinib and trigger avoidance for mast cell activation syndrome presenting with attacks of abdominal pain, nausea, vomiting, and diarrhea. ACG Case Rep J. 2024, 11:e01383. 10.14309/crj.0000000000001383
- Triggers of mast cell activation. (2024). Accessed: June 23, 2025: https://www.eds.clinic/articles/triggers-of-mcas-and-mcad.
- Woods JA, Vieira VJ, Keylock KT: Exercise, inflammation, and innate immunity. Immunol Allergy Clin North Am. 2009, 29:381-93. 10.1016/j.iac.2009.02.011
- Ernst AM, Schimak E, Steiner M, Lipp AT, Bauer HC, Bauer H: Lipedema adipocytes in culture: signs of hypertrophy, inflammation, and fibrosis. Adipose Tissue Homeostasis in Health and Disease. IntechOpen, 2024. 10.5772/intechopen.1004241
- Bonetti G, Michelini S, Donato K, et al.: Targeting mast cells: sodium cromoglycate as a possible treatment of lipedema. Clin Ter. 2023, 174:256-62. 10.7417/CT.2023.2496
- Amato AC, Benitti DA: Lipedema can be treated non-surgically: a report of 5 cases. Am J Case Rep. 2021, 22:e934406. 10.12659/AJCR.934406
- Choi YH, Yan GH, Chai OH, Song CH: Inhibitory effects of curcumin on passive cutaneous anaphylactoid response and compound 48/80-induced mast cell activation. Anat Cell Biol. 2010, 43:36-43. 10.5115/acb.2010.43.1.36
- Zhu TH, Zou G, Ding SJ, et al.: Mast cell stabilizer ketotifen reduces hyperalgesia in a rodent model of surgically induced endometriosis. J Pain Res. 2019, 12:1359-69. 10.2147/JPR.S195909
- Jihwaprani MC, Rizky WC, Mushtaq M: Pharmacokinetics of quercetin. Quercetin – Effects on Human Health. IntechOpen, 2023. 10.5772/intechopen.1003172
- Mlcek J, Jurikova T, Skrovankova S, Sochor J: Quercetin and its anti-allergic immune response. Molecules. 2016, 21:623. 10.3390/molecules21050623
- Weng Z, Zhang B, Asadi S, et al.: Quercetin is more effective than cromolyn in blocking human mast cell cytokine release and inhibits contact dermatitis and photosensitivity in humans. PLoS One. 2012, 7:e33805. 10.1371/journal.pone.0033805
- Alkuperäinen teksti: Association Between Hormonal Contraceptive Use and Lipedema: A Cross-Sectional Study With 637 Brazilian Women | Cureus
